Что такое дефект межпредсердной перегородки (ДМПП)?
Какие причины возникновения ДМПП известны?
Какие симптомы характерны для дефекта межпредсердной перегородки?
Каким образом можно поставить диагноз ДМПП?
Какие способы лечения ДМПП у детей и у взрослых используются в настоящее время?
Какие виды операций используются при лечении ДМПП?
Какие препараты могут использоваться при лечении дефекта межпредсердной перегородки?
Как необходимо восполнять дефицит питания у детей с ДМПП?
Как протекает послеоперационный период после операции закрытия дефекта межпредсердной перегородки?
Каков прогноз после операции по поводу дефекта межпредсердной перегородки?
Возможна ли профилактика развития ДМПП и что родителям необходимо сделать при выявлении диагноза у ребенка?
Что такое дефект межпредсердной перегородки (ДМПП)?
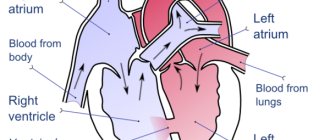
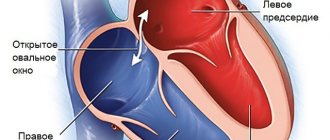
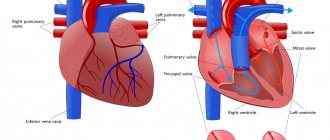
Дефект межпредсердной перегородки представляет собой патологическое отверстие в мышечной стенке, расположенной между двумя предсердиями (верхними камерами) сердца. В процессе эмбрионального развития для осуществления правильного кровообращения в сердце формируется отверстие между правым и левым предсердиями. Его также называют открытым овальным окном и необходимо оно для уравновешивания потоков крови в большом и малом круге кровообращения ребенка, поскольку из-за отсутствия дыхания и газообмена малый круг неактивен в достаточной степени. Обычно оно самостоятельно зарастает непосредственно перед родами. Но в некоторых случаях открытое овальное окно или, если оно имеет больший размер, дефект межпредсердной перегородки сохраняется и вызывает патологический сброс крови из левого предсердия в правое или происходит так называемое шунтирование крови.
В зависимости от расположения дефекта в межпредсердной перегородке, выделяют несколько вариантов ДМПП. Чаще всего патологическое сообщение между предсердиями располагается в центре или середине межпредсердной перегородки, что по статистике составляет более 70% всех случаев ДМПП. Согласно классификации ДМПП выделяют еще 4 формы дефектов:
- патологическое отверстие формируется в верхней части перегородки в области впадения в правое предсердие верхней полой вены, которая также называется дефектом межпредсердной перегородки венозного синуса;
- в нижней части перегородки, в области впадения нижней полой вены;
- в самой нижней части перегородки между предсердиями непосредственно над желудочками и называется первичным ДМПП;
- множественные дефекты межпредсердной перегородки.
В зависимости от расположения этих патологических сообщений возможно их влияние на внутрисердечное кровообращение. Так например, ДМПП венозного синуса может вовлекать в процесс правую верхнюю легочную вену, а первичный ДМПП часто выявляется в комбинации с нарушением строения митрального клапана и/или трикуспидального клапана сердца и вызывает регургитацию (обратный ток крови) через эти клапаны. В некоторых случаях возможно формирование комбинированного врожденного порока сердца, например комбинации с дефектом межжелудочковой перегородки. ДМПП у детей могут быть как небольшого точечного размера, так и больших размеров с вовлечение практически всей перегородки.
Дефекты межпредсердной и межжелудочковой перегородок являются наиболее распространенными врожденными пороками сердца. На долю ДМПП у детей приходится около 4-10% всех врожденных пороков сердца в Соединенных Штатах Америки. Дефект межпредсердной перегородки в 2 раза чаще выявляется у женщин.
Рис.1 Наиболее распространенные виды ДМПП у детей (объяснение в тексте)
Врожденные аномалии [пороки развития] сердечной перегородки (Q21)
Исключен: приобретенный дефект сердечной перегородки (I51.0)
Дефект коронарного синуса
Незаращенное или сохранившееся:
- овальное отверстие
- вторичное отверстие (тип II)
Дефект венозного синуса
Общий атриовентрикулярный канал
Дефект эндокарда в области основания сердца
Дефект первичного отверстия предсердной перегородки (тип II)
Дефект межжелудочковой перегородки со стенозом или артезией легочной артерии, декстропозицией аорты и гипертрофией правого желудочка.
Дефект аортальной перегородки
Дефект Эйзенменгера (Eisenmenger’s defect)
Дефект перегородки (сердца) БДУ
В России Международная классификация болезней 10-го пересмотра (МКБ-10) принята как единый нормативный документ для учета заболеваемости, причин обращений населения в медицинские учреждения всех ведомств, причин смерти.
МКБ-10 внедрена в практику здравоохранения на всей территории РФ в 1999 году приказом Минздрава России от 27.05.97г. №170
Выход в свет нового пересмотра (МКБ-11) планируется ВОЗ в 2017 2018 году.
https://www.youtube.com/watch?v=kEGKCuI0ni4
С изменениями и дополнениями ВОЗ гг.
РЦРЗ (Республиканский центр развития здравоохранения МЗ РК)
Версия: Клинические протоколы МЗ РК
Врождённые пороки сердца — одна из наиболее частых аномалий развития, занимающая третье место после аномалий центральной нервной системы и опорно-двигательного аппарата. Рождаемость детей с врождёнными пороками сердца во всех странах мира составляет от 2,4 до 14,2 на 1000 новорождённых. Частота встречаемости врождённых пороков сердца среди живорождённых составляет 0.
7-1,2 на 1000 новорождённых. Пороки с одинаковой частотой встречаемости нередко по-разному представлены в нозологической структуре среди больных, поступающих в кардиологические отделения (например, небольшой дефект межпредсердной перегородки и тетрада Фалло). Это связано с различной степенью угрозы для здоровья или жизни ребёнка.
Проблемы диагностики и лечения врождённых пороков сердца чрезвычайно важны в детской кардиологии. Терапевты и кардиологи, как правило, недостаточно знакомы с этой патологией в силу того, что подавляющее большинство детей к половозрелому возрасту подвергаются оперативному лечению или погибают, не получив своевременной адекватной помощи.
Причины возникновения врождённых пороков сердца неясны. Наиболее уязвимый периоднед беременности, то есть время, когда происходит закладка и формирование структур сердца. Большое значение имеют тератогенные факторы внешней среды, заболевания матери и отца, инфекции, особенно вирусные, а также алкоголизм родителей, приём наркотических веществ, курение матери. Ассоциированы с врождёнными пороками сердца многие хромосомные заболевания.
Анатомо-морфологическая тяжесть, т.е. вид патологии. Выделяют следующие прогностические группы:
- врождённые пороки сердца с относительно благоприятным исходом: открытый артериальный проток, дефект межжелудочковой перегородки (ДМЖП), дефект межпредсердной перегородки (ДМПП), стеноз лёгочной артерии; при этих пороках естественная смертность на первом году жизни составляет 8-11%;
- тетрада Фалло, естественная смертность на первом году жизни%;
- сложные врождённые пороки сердца: гипоплазия левого желудочка, атрезия лёгочной артерии, общий артериальный ствол; естественная смертность на первом году жизни — от 36-52% до 73-97% .
- Возраст больного на момент манифестации порока (появления клинических признаков гемодинамических нарушений).
- Наличие других (экстракардиальных) пороков развития, увеличивающих смертность у трети детей с ВПС до 90%.
- Масса тела при рождении и недоношенность.
- Возраст ребёнка к моменту коррекции порока.
- Тяжесть и степень гемодинамических изменений, в частности — степень лёгочной гипертензии.
- Вид и вариант кардиохирургического вмешательства.
Без оперативного лечения врожденные пороки сердца протекают по-разному. Например, у детей в возрасте 2-3 нед синдром гипоплазии левого сердца или атрезию лёгочной артерии (с интактной межпредсердной перегородкой) отмечают редко, что связано с высокой ранней смертностью при таких пороках. Суммарная летальность при врожденных пороках сердца высока.
К концу первой недели умирают 29% новорождённых, к первому месяцу — 42%, к первому году — 87% детей. С учётом современных возможностей кардиохирургической помощи практически при всех врожденных пороках сердца возможно проведение операции новорождённому. Однако не все дети с врожденными пороками сердца нуждаются в оперативном лечении сразу после выявления патологии.
С учётом тактики лечения пациенты с врожденными пороками сердца разделены на три группы:
- пациенты, для которых операция по поводу врожденных пороков сердца необходима и возможна (около 52%);
- пациенты, которым операция не показана из-за незначительности нарушений гемодинамики (около 31%);
- пациенты, для которых невозможна коррекция врожденных пороков сердца, а также неоперабельные по соматическому состоянию (около 17%).
Перед врачом, заподозрившим врожденный порок сердца, стоят следующие задачи:
- выявление симптомов, свидетельствующих о наличии ВПС;
- проведение дифференциальной диагностики с другими заболеваниями, имеющими сходные клинические проявления;
- решение вопроса о необходимости срочной консультации специалиста (кардиолога, кардиохирурга);
- проведение патогенетической терапии.
Существует более 90 вариантов врожденных пороков сердца и множество их сочетаний.
При опросе родителей следует уточнить сроки становления статических функций ребёнка: когда начал самостоятельно сидеть в кроватке, ходить. Необходимо выяснить, как ребёнок прибавлял в весе на первом году жизни, поскольку сердечная недостаточность и гипоксия, сопутствующие порокам сердца, сопровождаются повышенной утомляемостью, «ленивым» сосанием и плохой прибавкой массы.
Пороки с гиперволемией малого круга кровообращения могут сопровождаться частыми пневмониями и бронхитами. При подозрении на порок с цианозом следует уточнить сроки появления цианоза (с рождения или в течение первого полугодия жизни), при каких обстоятельствах появляется цианоз, его локализацию. Кроме того, при пороках с цианозом всегда бывает полицитемия, что может сопровождаться расстройствами со стороны центральной нервной системы, такими, как гипертермия, гемипарезы, параличи.
Телосложение
Изменение телосложения бывает при немногих пороках. Так, коарктация аорты сопровождается формированием «атлетического» телосложения, с преобладанием развития плечевого пояса. В большинстве же случаев для врожденных пороков сердца характерно пониженное питание, часто до 1-и степени гипотрофии, и/или гипостатура.
Возможно формирование таких симптомов, как «барабанные палочки» и «часовые стёкла», что характерно для врожденных пороков сердца синего типа.
Кожные покровы
При пороках бледного типа — бледность кожных покровов, при пороках с цианозом — диффузный цианоз кожи и видимых слизистых, с преобладанием акроцианоза. Однако насыщенная «малиновая» окраска концевых фаланг характерна и для высокой лёгочной гипертензии, сопровождающей пороки с лево-правым сбросом крови.
Дыхательная система
Изменения со стороны дыхательной системы часто отражают состояние усиленного лёгочного кровотока и проявляются на ранних этапах одышкой, признаками диспноэ.
При осмотре определяется «сердечный горб», расположенный бистернально или слева. При пальпации — наличие систолического или диастолического дрожания, патологического сердечного толчка. Перкуторно — изменение границ относительной тупости сердца. При аускультации — в какую фазу сердечного цикла выслушивается шум, его продолжительность (какую часть систолы, диастолы занимает), изменяемость шума при перемене положения тела, проводимость шума.
Изменения артериального давления (АД) при ВПС бывают нечасто. Так, для коарктации аорты характерно повышение АД на руках и значительное понижение на ногах. Однако подобные изменения АД могут быть и при сосудистой патологии, в частности, при неспецифическом аортоартериите. В последнем случае возможна значительная асимметрия АД на правой и левой руке, на правой и левой ноге. Понижение АД может быть при пороках с выраженной гиповолемией, например, при аортальном стенозе.
При ВПС возможно увеличение печени, селезёнки вследствие венозного застоя при сердечной недостаточности (обычно не более чем на 1,5-2 см). Венозное полнокровие сосудов брыжейки, пищевода может сопровождаться рвотой, чаще при физической нагрузке, и болями в животе (из-за растяжения печёночной капсулы).
Существует несколько классификаций врождённых пороков сердца.
Международная классификация болезней 10-го пересмотра. Врожденные пороки сердца относятся к разделу Q20-Q28. Классификация болезней сердца у детей (ВОЗ, 1970) с кодами «SNOP» (систематическая номенклатура патологии), используемая в США, и с кодами «ISC» Международного общества кардиологов.
Классификация врождённых пороков сердца и сосудов (ВОЗ, 1976), содержащая раздел «Врождённые аномалии (пороки развития)» с рубриками «Аномалии луковицы сердца и аномалии закрытия сердечной перегородки», «Другие врождённые аномалии сердца», «Другие врождённые аномалии системы кровообращения».
Создание единой классификации представляет определённые трудности в связи с большим количеством видов врожденных пороков сердца, а также с различием принципов, которые могут быть положены в основу классификации. В Научном центре сердечно-сосудистой хирургии им. А.Н. Бакулева была разработана классификация, в которой врожденные пороки сердца разделены по группам с учётом анатомических особенностей и гемодинамических нарушений. Предложенная классификация удобна для использования в практической деятельности. В данной классификации все ВПС разделены на три группы:
- ВПС бледного типа с артериовенозным шунтом, т.е. со сбросом крови слева направо (ДМЖП, ДМПП, открытый артериальный проток);
- ВПС синего типа с веноартериальным сбросом, т.е. со сбросом крови справа налево (полная транспозиция магистральных сосудов, тетрада Фалло);
- ВПС без сброса, но с препятствием к выбросу из желудочков (стеноз лёгочной артерии, коарктация аорты).
Какие причины возникновения ДМПП известны?
Причиной формирования дефекта межпредсердной перегородки являются особенности эмбрионального развития сердца. Четко выделить причины, почему это возникает и какой из факторов может на этот процесс повлиять сложно, но в большинстве случаев эксперты сходятся во мнении, что виной появления ДМПП являются генетический, экологический, физический и инфекционный факторы. В случаях если ДМПП оказывается маленьким и отсутствуют симптомы, он может остаться вообще не замеченным как для самого пациента, так и для врачей. Если же дефект оказывается больших размеров, обогащенная кислородом кровь из левого предсердия поступает в правое и дальше обратно в легкие. Сердцу приходится перекачивать дополнительное количество крови и выполнять «ненужную» работу. В результате такой нагрузки правые отделы сердца могут увеличиться в размерах и может возникнуть сердечная недостаточность.
В некоторых случаях, открытое овальное окно или дефект межпредсердной перегородки могут стать причиной перемещения тромбов из правой половины сердца в левую, в результате чего может возникнуть миграция этого тромба из сердца в головной мозг с последующим развитием инсульта. Если не заниматься лечением ДМПП, то возможно развитие его осложненного течения с появлением симптомов легочной гипертензии, инфекции легких, синдрома Эйзенменгера, фибрилляции предсердий, трепетания предсердий, инсульта или правосторонней сердечной недостаточности.
Аномалии развития сердца малые
Аномалии развития сердца малые: Краткое описание
Малые аномалии развития сердца (МАРС) — анатомические врождённые изменения сердца и магистральных сосудов, не приводящие к грубым нарушениям функций ССС. Ряд МАРС имеет нестабильный характер и с возрастом исчезает.
Этиология
Наследственно детерминированная соединительнотканная дисплазия. Ряд МАРС имеют дизэмбриогенетический характер. Не исключается воздействие различных экологических факторов (химическое, физическое воздействие).
Код по международной классификации болезней МКБ-10:
- Q20. 9 — Врожденная аномалия сердечных камер и соединений неуточненная
Какие симптомы характерны для дефекта межпредсердной перегородки?
Из-за хороших компенсаторных возможностей или небольшого диаметра дефекта межпредсердной перегородки симптомы ДМПП могут вообще отсутствовать вплоть до вступления во взрослую жизнь. Одним из первых симптомов ДМПП в таком случае бывает замедление физического развития ребенка по сравнению со сверстниками. Среди других симптомов, которые также появляются не сразу можно выделить следующие:
- одышка
- общая немотивированная слабость
- нарушение ритма сердца (артимия) или эпизоды трепетания сердца,
- переутомление при физической нагрузке, необходимость остановки во время тренировки или выполнения физических упражнений
- появление затруднения дыхания во время упражнений или физической активности
Необходимо отметить, что чем старше становится пациент, тем интенсивнее становится выраженность этих симптомов ДМПП (конечно же при отсутствии других заболеваний).
При каких симптомах ДМПП необходимо вызвать врача?
Есть ряд состояний, при которых родителям ребенка необходимо вызвать на дом педиатра или детского кардиолога:
- припухлость или отек в области лодыжек и голеней
- увеличение в размерах живота
- непереносимость физической нагрузки и упражнений
- часто возникающие и хронические бронхиты и инфекции дыхательных путей
- изменение нормального артериального давления
- присоединение симптомов системной инфекции в организме, включая ангину, ломоту в теле или лихорадку
Иногда состояние ребенка может ухудшиться и потребуется оказание специализированной помощи. Вот некоторые из состояний, при которых родителям ребенка необходимо будет вызвать скорую медицинскую помощь или бригаду «03» для госпитализации ребенка в профильное отделение:
- выраженное затруднение дыхания или одышка, появление быстрого поверхностного дыхания
- головокружение или резкая слабость
- постоянный кашель или кашель с примесью или прожилками крови
- синюшный тон кожи или синюшность вокруг губ, ногтей и языка
- нарушение ритма сердца (аритмия) или трепетания сердца,
- боль в грудной клетке (у детей встречается редко)
Клиническая картина опасного состояния
В самом начале своего развития аномалия не сопровождается никакими признаками, и не проявляет себя. Далее её симптомы чаще всего связаны с возрастом:
- от 1 года до 3 лет: обратить внимание следует на появление некоторого отставания в физическом развитии малыша, он может не успевать набирать нужный вес, быть слишком восприимчивым к вирусным инфекциям;
- от 4 до 7 лет: ребенок не выдерживает физическую нагрузку, жалуется на слабость, боли в груди, отстает в росте. Наблюдается бледность кожных покровов, аритмии;
- после 7 лет: дети этого возраста также отстают в физическом развитии, может наблюдаться задержка в развитии половой системы, боли в груди. При прослушивании врач слышит характерные аномалии негромкие систолические шумы.
- резко возникшую боль в груди;
- ощущение дискомфорта;
- повышенную слабость;
- неспособность справляться с любыми физическими нагрузками.
Каким образом можно поставить диагноз ДМПП?
Большую информацию о возможном наличии врожденного порока сердца в общем и дефекта межпредсердной перегородки в частности, позволяет получить тщательный сбор семейного анамнеза врожденной патологии у ближайших родственников. Наличие в анамнезе ВПС у родителей, братьев или сестер позволяет предположить существование генетической предрасположенности. Уже на приеме у детского кардиолога можно установить предварительный диагноз. Для этого кардиолог осмотрит ребенка, измерит артериальное давление и проведет аускультацию (выслушивание) сердца и легких с помощью стетоскопа. Аускультация позволит выслушать в сердце патологические шумы, обусловленные неправильным потоком крови, возникающим при наличии дефекта межпредсердной перегородки. Во время осмотра кардиолог также оценит характеристики пульса, рефлексы, рост и вес малыша, что позволит выявить возможные нарушения ритма сердца и физического развития. Поскольку возникающее при ДМПП нарушение кровообращения часто характеризуется изменением обогащения крови кислородом, ребенку проведут измерение насыщения крови кислородом, для чего разместят на кончик пальца или мочку уха прибор, называемый пульсоксиметром. Также при осмотре кардиолог может провести пальпацию (ощупывание) внутренних органов, для того чтобы определить есть ли их увеличение или болезненность.
Комплексная диагностика ДМПП включает также проведение таких методов исследования как рентген грудной клетки, электрокардиография (ЭКГ, кардиограмма), эхокардиография (ЭхоКГ) или магнитно-резонансная томография (МРТ), которые могут подтвердить наличие дефекта в межпредсердной перегородке. С помощью рентген грудной клетки проводят оценку размеров, формы и местоположения сердца и легких.
ЭКГ отображает электрическую активность сердца. Во время ЭКГ исследования к поверхности кожи на передней поверхности груди присоединяют специальные маленькие электроды в виде присосок. Эти электроды проводами связаны с электрокардиографом, который распознает и записывает в виде кривой на бумаге электрические импульсы, возникающие в сердце в разные стадии его сократительной активности.
Принцип работы ЭхоКГ заключается в использовании диагностических свойств ультразвука или высокочастотных звуковых волн, с помощью которых возможен компьютерный анализ и построение изображения внутренних структур сердца. С помощью ЭхоКГ с высокой степенью достоверности и точности можно определить любую патологию структур сердца (клапанов, камер, крупных сосудов и т.д.). Если ЭхоКГ проводится в комбинации с допплерографией, возможно изучение характера потоков крови, возникающих в полостях сердца и при прохождении через клапанные структуры.
Эхокардиография при дефекте межпредсердной перегородки (видео)
Магнитно-резонансная томография – метод исследования, предполагающий использования энергии магнитного поля и возникающих под его влиянием радиоволн, что позволяет воссоздать трехмерную (3D) картину строения сердца, а использование во время МРТ-исследования динамического режима позволяет понять насколько эффективно работает сердца и как происходит циркуляция крови внутри сердца и крупных сосудов.
В случае необходимости проведения дополнительной диагностики или определения тактики лечения ДМПП ребенка госпитализируют в кардиохирургический центр и уже в стационарных условиях проводят процедуру, которая называется сердечным зондированием. Этот метод исследование более агрессивный, чем озвученные ранее, поскольку предполагает выполнение пункции сосудов и введение в просвет сосуда и полостей сердца специальных эндоваскулярных (внутрисосудистых) устройств. Сердечное зондирование является «золотым стандартом» постановки диагноза ДМПП при планировании хирургического лечения. Обычно оно выполняется в условиях крупного, технически хорошо оснащенного кардиохирургического стационара, который имеет огромный опыт проведения подобных процедур и высококвалифицированный штат сотрудников. Во время сердечного зондирования в просвет вены или артерии, путем пункции вводится длинная пластиковая эластическая трубочка, называемая катетером, и продвигается в направлении сердца под контролем рентгенографической установки. После достижения зоны предполагаемого исследования (например, область межпредсердного сообщения при ДМПП) для улучшения качества снимка и прокрашивания сосудистого русла и полостей сердца, в просвет вводится рентгеноконтрастный материал (контраст), с последующей регистрацией изображения с помощью рентгеновского аппарата и записью результата на видео. Такую технику исследования также называют ангиографией. Катетер позволяет также произвести измерение давление внутри полостей сердца, а также определить насыщение полученной из разных камер сердца крови. Например, если между предсердиями есть сообщение, то кровь обогащенная кислородом из левого предсердия попадает в правое, смешиваясь там с обедненной кислородом венозной кровью. Увеличение насыщения крови в правых отделах (предсердии и желудочке) сердца косвенно будет указывать на наличие такого патологического сообщения между правыми и левыми камерами сердца.
Диагностика
Проверить состояние и работу сердца, выявить заболевание позволяют следующие методы исследования:
- Электрокардиограмма (ЭКГ). Позволяет определить перегруженность сердечных желудочков, выявить наличие и степень гипертензии легких;
- Фонокардиография (ФКГ). В результате исследования возможно выявление шумов сердца;
- Эхокардиография (ЭхоКГ). Способно выявлять нарушения кровотока и помогает подозревать дмжп;
- Ультразвуковое исследование. Помогает оценить работу миокарда, уровень давления артерии легкого, количество сбрасываемой крови;
- Рентгенография. По снимкам грудной клетки возможно определение изменений легочного рисунка, увеличение размеров сердца;
- Зондирование сердца. Позволяет определить уровень давления в артерии легких и желудочке сердца, повышенное содержание кислорода в венозной крови;
- Пульсоксиметрия. Помогает выяснить уровень содержания кислорода в крови – недостаток говорит о нарушениях в сердечно-сосудистой системе;
- Катетеризация сердца. Помогает оценить состояние структуры сердца, выяснить уровень давления в сердечных желудочках.
Какие способы лечения ДМПП у детей и у взрослых используются в настоящее время?
Как показали статистические исследование приблизительно у 20% детей, имеющих дефект межпредсердной перегородки, к возрасту 2 лет дефект закрывается самостоятельно без проведения лечения. В случаях если самостоятельного закрытия ДМПП не происходит обычно предпринимают оперативное лечение, поскольку дальнейшее сохранение дефекта чревато формированием утолщения стенок легочной артерии и легочной гипертензии. Если своевременно не прибегнуть к лечению ДМПП возможно развитие необратимого состояния, которое также называется хронической обструктивной болезнью легочных артерий, риск неблагоприятного исхода увеличивается на 25%. Первый этап лечения ДМПП у детей обычно проводится детским кардиологом, имеющим большой опыт диагностики и лечения врожденных пороков сердца. Он предполагает проведение поддерживающей терапии и позволяет справиться с возникшими нарушениями кровообращения и сердечной недостаточности, а также подготовить ребенка к операции. Операция по поводу этого порока обычно проводится опытным детским сердечно-сосудистым хирургом, имеющим большой опыт проведения операций по закрытию и пластике ДМПП. Различного рода эндоваскулярные вмешательства при лечении дефекта межпредсердной перегородки выполняются интервенционным кардиологом или детским эндоваскулярным кардиохирургом.
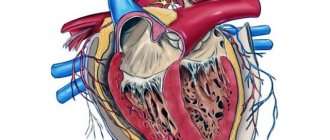
Рис.2 Варианты операция при ДМПП (вверху — закрытие дефекта окклюдером; внизу — пластика заплатой)
Какие виды операций используются при лечении ДМПП?
Открытая операция ДМПП
Существует 2 основных варианта закрытия ДМПП во время операции: первый используется при небольшом размере ДМПП и предполагает наложение одного шва для сближения и сопоставления краев этого дефекта; во время второго варианта проводится пластика ДМПП с помощью заплаты и суть ее состоит в замещении области дефекта синтетическим материалом (обычно это заплата из дакрона) или собственными тканями (чаще для этого используется заплата из перикарда или специально обработанного перикарда, называемого ксеноперикардом).
Во время традиционного хирургического вмешательства по закрытию ДМПП доступ к сердце выполняется либо средней линии грудины с ее последующим разведением (доступ носит название стернотомии), либо в одном из межреберных промежутков (доступ носит название торакотомии). После специальном подготовки сердце подключают аппарату искусственного кровообращения (аппарат сердце-легкие), охлаждают и останавливают сердце, и далее выполняют пластику ДМПП уже в условиях неподвижного и «сухого» бескровного сердца, что необходимо для выполнения высокоточной хирургической работы. Сроки выздоровления после такого варианта лечения дефекта межпредсердной перегородки обычно составляет 5-7 дней, а сроки реабилитации в домашних условиях после выписки из больницы 4-6 недель. В настоящее время, для сокращения сроков выздоровления и реабилитации, уменьшения размеров рубцов используются минимально инвазивная техника операций с использованием небольших доступом до 7-10 см в длину. Доступ обычно выбирается в зависимости от размера ДМПП и его месторасположения. Выполнение операции при бессимптомном течении заболевания обычно рекомендуют за 1-2 года до школы. При наличии симптомов и замедлении физического развития ребенка, рекомендуется провести лечение дефекта межпредсердной перегородки как можно раньше, до появления вторичных изменений в сердце и легких.
Эндоваскулярное закрытие ДМПП окклюдером
У операции эндоваскулярного закрытия ДМПП есть несколько преимуществ перед традиционной открытой операцией, что делает ее все более востребованной и используемой в качестве альтернативы. Прежде всего эндоваскулярное лечение дефекта межпредсердной перегородки у детей не требует выполнения широкого травматичного доступа и использования во время операции аппарата искусственного кровообращения. Как результат это приводит к снижению сроков пребывания в больнице, отсутствию больших рубцов после операции, сокращает сроки выздоровления и реабилитации. После эндоваскулярного закрытия ДМПП ребенок остается в стационаре на одни, максимум двое суток, и в течение 1-2 недель происходит его полное восстановление и возвращение к обычному режиму активности.
В основе процедуры эндоваскулярного лечения лежит своеобразное закупоривание патологического сообщения между предсердиями специальным устройством, которое носит название окклюдера. Однако установка окклюдера при ДМПП не всегда выполнима. Существует ряд клинических ситуаций, при которых этот вариант лечения дефекта межпредсердной перегородки не совсем подходит, а именно в случаях, когда сообщение между предсердиями слишком больших размеров или расположено не в центре межпредсердной перегородки или же ткани перегородки недостаточно для прочной фиксации окклюдера. Существует еще ряд противопоказаний к закрытию ДМПП с помощью окклюдера: резкое сужение сосудов и неспособность доставки окклюдера к месту имплантации; патология клапанов сердца, когда необходима коррекция этой патологии; патологический венозный дренаж из легких; наличие инфекции клапанов; наличие тромбов в просвете камер сердца или нарушения гемостаза (системы свертывания и противосвертывания крови) или непереносимость аспирина или аспириноподобных препаратов.
Принцип эндоваскулярного закрытия ДМПП у детей (видео)
Именно поэтому перед планированием лечения дефекта межпредсердной перегородки проводят точную диагностику с определением точного размера и местоположения дефекта. Накануне процедуры закрытия ДМПП окклюдером назначают курс антикоагулянтной и дезагрегантной терапии, повышающих текучесть крови и снижающих возможность образования тромба. Окклюдер перед установкой размещен фирмой производителей специальном катетере, который после пункции бедренной вены перемещается к месту расположения ДМПП. После чего проводится имплантация устройства в дефект и он остается там постоянно, предотвращает смешивание разных потоков крови между двумя предсердиями. С целью определения правильного расположения и позиции окклюдера выполняют контрольную ангиографию. В течении 24 часов выполняются контрольные ЭКГ и ЭхоКГ исследования, а также рентген грудной клетки, также подтверждающие правильное расположение окклюдера. В последующем, в отдаленном периоде после операции закрытия ДМПП, происходит прорастание собственной ткани миокарда в устройство и оно становится частью перегородки сердца. Несмотря на то, что окклюдер имеет четкие размеры и не увеличивается со временем, при росте ребенка происходит также рост ткани покрывающей устройство.
Классификация
Дефект межжелудочковой перегородки у новорожденных и детей постарше может диагностироваться как самостоятельная проблема (изолированный порок), так и как составная часть других сердечно-сосудистых заболеваний, например, пентады Кантрелла (кликните сюда, чтобы почитать о ней).
Размер дефекта оценивается исходя из его величины по отношению к диаметру аортального отверстия:
- дефект размером до 1 см классифицируется как малый (болезнь Толочинова-Роже);
- крупными считаются дефекты от 1 см или те, которые по своим размерам превышают половину устья аорты.
Наконец, по локализации отверстия в перегородке ДМЖП делится на три типа:
- Мышечный дефект межжелудочковой перегородки у новорожденного. Отверстие располагается в мышечной части, в отдалении от проводящей системы сердца и клапанов, и при небольших размерах может закрываться самостоятельно.
- Мембранозный. Дефект локализируется в верхнем сегменте перегородки ниже аортального клапана. Обычно он имеет небольшой диаметр и купируется самостоятельно по мере роста ребенка.
- Надгребневый. Считается самым сложным видом порока, так как отверстие в этом случае находится на границе выводящих сосудов левого и правого желудочка, и самопроизвольно закрывается очень редко.
Какие препараты могут использоваться при лечении дефекта межпредсердной перегородки?
Для пациентов после операции обычно назначают дезагреганты и антикоагулянты, например аспирин или варфарина (Coumadin) в течение трех — шести месяцев после выполнения процедуры. Поскольку окклюдер является инородным предметом, это лечение необходимо для профилактики формирования тромбов вокруг устройства.
Мочегонные средства (диуретики) назначают при выявлении симптомов сердечной недостаточности и задержке в организме жидкости и отеках. Диуретики способствуют выделению избыточной жидкости и солей. Поскольку при терапии диуретиками возможны потери калия, в комбинации с диуретиками назначают калийсодержащие препараты (Аспаркам). Для увеличения сократительной активности сердца назначают дигоксин, который также способен снижать частоту сердцебиений, удалять избыток жидкости из тканей и обладает гипотензивным эффектом при высоком артериальном давлении.
Лечение
Включает в себя три задачи. Купирование симптомов, устранение самого дефекта, а также предотвращение осложнений, потенциально смертельных. Все решают в один и тот же момент.
При небольшом дефекте МЖП, независимо от возраста пациента, если отсутствуют выраженные нарушения, аритмии, прочие симптомы, к тому же состояние не прогрессирует, выбирают выжидательную тактику.
Каждые несколько месяцев оценивают объективные показатели, при наличии негативного течения показана операция.
Проводят ее планово
До хирургического вмешательства важно подготовить пациента, стабилизировать его состояние медикаментозными методами
Конкретные наименования препаратов зависят от возраста больного и уровня функциональных нарушений.
Как правило, показаны такие средства:
- Противогипертензивные. Ограничиваются бета-блокаторами для купирования повышенного артериального давления и устранения тахикардии.
- Кардиопротекторы. Восстанавливают обмен веществ в сердце.
- Медикаменты на основе калия и магния. Питают миокард, нормализуют сократительную способность.
Продолжительность подготовительного периода — около 2-3 месяцев, больше крайне редко.
Само оперативное вмешательство заключается в ушивании дефекта (с рассечением грудной клетки), или восстановлении анатомической целостности тканей с помощью окклюдера (без рассечения грудины).
Реабилитационный период продолжается примерно полгода. Значительных ограничений в дальнейшей жизни нет. Если патология устранена, все возвращается в норму.
Как необходимо восполнять дефицит питания у детей с ДМПП?
Новорожденные и дети с ДМПП всегда очень медленно набирают в весе, и наиболее распространенной причиной такого плохого роста является избыточное выделение тепловой энергии или ее недостаточное поступление с питанием. Среди других факторов, которые часто являются причиной нарушения физического развития и избыточного расходования энергии детей с ДМПП, можно выделить следующие:
- учащенное сердцебиение и увеличение частоты дыхания
- плохой аппетит
- частые респираторные инфекции
- сниженное поглощение питательных веществ пищеварительным трактом
- снижение насыщения крови кислородом
Одной из особенностей питания новорожденных является то, что ребенок с ДМПП быстро переутомляется во время кормления. Педиатры рекомендуют в первые два месяца после рождения кормить ребенка каждые два часа малыми порциями и кормление необходимо производить только по требованию. У некоторых новорожденных нарушение питания может быть связано с особенностями строения бутылочки для кормления, поэтому родители должны подобрать наиболее подходящий для ребенка вариант. Если ребенку прописаны лекарственные препараты, лучше принимать их перед питанием и важно чтобы не происходило смешивания препарата и грудного молока или питательной смеси. Педиатр также должен будет сообщить родителям о сроках перевода на твердую пищу, ориентировочно это происходит на 6 месяц после рождения. Желательно в течение 2-х лет избегать приема пищи, содержащей жиры. Оптимальным для быстрого роста считается использование сбалансированных высококалорийных питательных смесей. При формировании диеты у детей старше 2-х лет, рекомендуются придерживаться следующих принципов питания:
- потребление жиров должно составлять менее 30% от общего количества калорий потребляемых в течение дня
- количество калорий, приходящихся на насыщенные жиры, должно составлять не более 8-10% от общего количества калорий потребляемых в сутки
- объем потребления холестерина должен быть не выше 300 мг/дл в день
Последовательный переход к использованию так называемой средиземноморской диеты позволит в дальнейшем предотвратить ранее развитие ишемической болезни сердца во взрослой жизни. Пищевые продукты должны преимущественно состоять из зерновых, овощей, фруктов, постного мяса и других продуктов с низким содержанием жиров и высоким содержанием сложных углеводов и белков. Желательно при приготовлении блюд исключить соль, а также избегать употребления соленых продуктов. Для этого необходимо исключить из рациона продукты быстрого питания (фаст фуд), консервированные продукты и замороженную пищу, в которой соль используется для увеличения сроков пригодности.
Как протекает послеоперационный период после операции закрытия дефекта межпредсердной перегородки?
Дети, перенесшие открытую операцию по поводу ДМПП или эндоваскулярное закрытие, обычно нуждаются в пожизненном наблюдении и контроле со стороны детского, а затем и взрослого кардиолога. Наряду со стандартными осмотрами, эти пациенты нуждаются в постоянных исследованиях состояния их сердца. Обычно регулярная диагностика состояния сердца проводится перед и после операции, а в дальнейшем при положительных результатах родители забывают о необходимости постоянного контроля, что не совсем правильно. Важно постоянно проходить профилактические осмотры, делать контрольные исследования и поддерживать тесный контакт с лечащим врачом, хирургом и кардиологом. Кроме того, для профилактики присоединения различных инфекций, связанных с ослаблением иммунитета организма после операции, можно рекомендовать проведение иммунизации, например иммунизации вакциной против гриппа.
Каков прогноз после операции по поводу дефекта межпредсердной перегородки?
Перспективы и прогнозы относительно получения хороших результатов лечения ДМПП за последние два десятилетия существенно улучшились. В настоящий момент пациенты с маленьким размером дефекта могут жить обычной жизнью с минимальными рекомендациями, однако как было сказано ранее пациенты с большими ДМПП требуют оперативного лечения. Выполнение эндоваскулярного закрытия сопровождается очень хорошими результатами, при проведении реконструктивных открытый операций результаты несколько похуже, однако в большей степени они обусловлены лечением уже запущенных форм заболевания и наличием сложных реконструкций. В настоящее время менее 1% пациентов с ДМПП, перенесших сложные реконструктивные вмешательства, не доживают до 45-летия. Также статистически подсчитано, что приблизительно 5-10% пациентов, оперированных в возрасте старше 40 лет погибают от осложнений хирургии, эти цифры еще раз подчеркивают необходимость раннего выявления и лечения дефекта межпредсердной перегородки. Несмотря на озвученные цифры, следует еще раз напомнить, что без хирургического лечения погибает практически четверть (25%) пациентов с ДМПП. Как показывает практика, при выполнении лечения ДМПП в возрасте до 20 лет практически гарантирует возвращение ребенку полноценной и нормальной жизни.