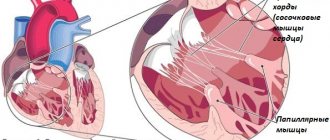
Кардиопротекторы — лекарственные средства, защищающие клетки сердца и улучшающие метаболические процессы в миокарде. Этот класс препаратов сравнительно молодой, поскольку появился на фармакологическом рынке в середине 90-х годов прошлого столетия.
Сердечной мышце регулярно необходим постоянный приток кислорода с кровью, с помощью которого происходят процессы фосфорилирования в тканях миокарда, нужные для поддержания правильной работы сердца. Низкий уровень насыщения тканей сердца кислородом (при ишемии) можно интерпретировать как нарушение баланса между скоростью транспорта крови, в которой содержится кислород, и потребностью в нём. Если клетки сердца не получают нужного количества кислорода, развивается ишемическая болезнь сердца (ИБС). У здоровых людей гипоксия тканей также возникает на фоне высокоинтенсивных физических нагрузок и психологического стресса. В результате этого функциональность сердечной мышцы снижается, и как следствие, развиваются симптомы стенокардии.
Отличным механизмом адаптации клеток сердца (кардиомиоцитов) является подстройка метаболических процессов под внешние факторы. На сегодняшний момент разработано и проверено большое количество препаратов-кардиопротекторов, максимально воздействующих на энергетические субстраты, а также на оптимизацию функций кардиореспираторной системы и на ускорение восстановительных процессов.
Основные факторы, которые учитывались при создании метаболических кардиопротекторов это: нормализация энергообмена в организме, накопление энергочастиц, экономный расход макроэргов, профилактика переутомления, адаптация сердечной мышцы к меняющимся условиям окружающей среды, защита клеток сердца от свободных радикалов, а также нормализация работы вегетососудистой системы и т.д.
Принципы воздействия подобного рода препаратов различны и многообразны. В нормальных условиях, при достаточном поступлении кислорода в ткани миокарда, сердечные миоциты снабжаются энергией из АТФ (аденозинтрифосфата) путём распада ацетилкофермента-А в цикле трикарбоновых кислот, а основным источником их энергоснабжения является глюкоза и жирные кислоты. При нормальном кровообращении в миокарде большая часть ацетилкофермента-А формируется через окислительные процессы с участием жирных кислот, а меньшая – через процесс декарбоксилирования пирувата. Приблизительно 50% от всего пирувата в клетках формируется путём расщепления глюкозы, остальные 50% — из молочной кислоты, проникающего внутрь клетки из крови. Катаболические процессы с участием свободных жирных кислот в отличие от процессов распада глюкозы (гликолиза) требуют наличия большого количества молекул кислорода для дальнейшей выработки АТФ (без кислорода синтез АТФ в данном случае не происходит). При нормальном уровне кислорода в клетках механизмы, отвечающие за расщепление глюкозы и окисление жиров находятся в состоянии баланса. При недостатке кислорода в клетках окисление жирных кислот подавляется, как следствие, митохондрии начинают кумулировать активизированные формы свободных жирных кислот (ацилкарнитин, ацилкофермент-а и пр.), способные угнетать АТФ-насос и замедлять транспортировку АТФ из митохондрий в цитоплазму и клеточную мембрану.
Нормализовать клеточный энергообмен можно за счёт:
- Увеличения эффективности работы митохондрий в состоянии гипоксии, вызванного нарушением окислительных процессов и нарушением фосфорилирования; сюда же можно отнести повышение прочности митохондриальных мембран;
- Ускорения цикла трикарбоновых кислот.
- Компенсации разрушенных биокомпонентов, участвующих в «дыхании» клеток;
- Образования новых окислительно-восстановительных процессов;
- Снижения клеточной потребности в кислороде и увеличения кислородного запаса;
- Повышения количества АТФ при липолитических процессах в процессе гликолиза (без повышения выработки молочной кислоты);
- Уменьшения расхода АТФ на «маловажные» процессы, не требующие экстренного реагирования внутриклеточных механизмов в критических состояниях;
- Введения искусственных макроэргов (энергетических единиц).
За счёт подобных эффектов кардиопротекторы можно подразделить по действию на прямые и непрямые. Влияние прямых кардиопротекторных препаратов объясняется их локальным (усиление прочности клеточных мембран, положительное воздействие на метаболические процессы в мышечных клетках сердца, вазодилатирующее действие) и общим влиянием на системы организма (нормализация тонуса сосудов через воздействие на ЦНС). Непрямые кардиопротекторы снижают нагрузку на сердце, что положительным образом сказывается на работе миокарда.
Подгруппы прямых кардиопротекторов
1.Средства, модулирующие энергообмен в сердечной мышце
- Лекарственные препараты с прямым влиянием на энергопроцессы – триметазидин, мексидол, таурин, мельдоний, аспаркам, «Kardioton»
- Нестероидные анаболики –, оротат калия, метилурацил, рибоксин, препараты с высоким содержанием магния, «Леветон Форте».
- Антиоксиданты – витамин Е, витамин В3 и С; кверцетин, танин и прочие флавоноиды.
- Вещества, препятствующие возникновению свободных радикалов – витамин В2, цитохром С, коферменты Q.
2.Активные вещества, воздействующие на баланс электролитов в миокарде
- Блокаторы кальциевых каналов избирательного действия – амлодипин, верапамил и пр.
- Ингибиторы натриевых каналов – карипозид и пр.
- Катализаторы АТФ-зависимых каналов.
3.Стабилизаторы клеточных оболочек миокарда
- Антиаритмические препараты – амиодарон, дизопирамид, соталол и пр.
4.Препараты, снижающие потребность сердечной мышцы в кислороде
- Нитраты – нитроглицерин и т.д.
- Бета-блокаторы – пропранолол, бисопролол, невиболол и пр.
- Блокаторы альфа- и бета-адренорецепторов – карведилол и пр.
- Натрийуретические пептиды
Подгруппы непрямых кардиопротекторов
1.Гипотензивные препараты с различным воздействием на организм.
- Мочегонные средства, защищающие миокард – индапамид, спиронолактон, фуросемид и т.д.
- Ингибиторы АПФ (ангиотензин-превращающего фермента) – эналаприл, периндоприл и пр.
- Сартаны (блокаторы ангиотензиновых рецепторов II) – вальсартан, эпросартан и пр.
2.Антикоагулирующие препараты
- Ингибиторы коагуляции тромбоцитов – аспирин, тиклоподин и пр.
- Антикоагулянты – варфарин, гепарин и пр.
3.Лекарства, воздействующие на обмен жиров
- Статины – симвастатин, аторвастатин и т.д.
- Ненасыщенные жирные кислоты – омега-3
Спортивные медики много внимания акцентируют на препараты, регулирующие метаболические процессы в сердечной мышце при низком содержании кислорода в крови и в тканях сердца. Прочие лекарственные препараты назначаются в период восстановления между тренировками, а также при развитии кардиологических патологий, обусловленных воздействием физических нагрузок.
Использование препаратов-кардиопротекторов с антигипоксическим эффектом обуславливается не только одним лишь представлением о защитных свойствах данного класса лекарств, но и наличием большого количества информации для специалистов, описывающей всей фармакологические свойства кардиопротекторов. Необходимо отметить, что использование такого рода средств может зависеть от вариативности тренировочных параметров. В особенности, использование кардиопротекторных субстратов, предотвращающих сердечную гипоксию, оправдано в период проведения соревнований. Антигипоксические препараты, как правило, применяются при постоянных физических нагрузках, которые увеличивают адаптации сердечно-сосудистой и дыхательной систем у спортсменов, показывающих высокий уровень выносливости в период состязаний.
Достаточно быстро купируют гипоксию в тканях антигипоксические субстраты. К таким веществам относят глютамин, аспарагин и янтарную кислоту. Однако полезность этих веществ при гипоксическом состоянии сердца не подтверждена клинически. По всей видимости, данный факт может быть связан с тем, что глютамин и янтарная кислота принимают участие в цикле трикарбоновых кислот с конечным образованием своих производных — альфа-кетоглутаровой кислоты и оксалоацетата, которые могут полностью восстанавливать структуру фумаровой кислоты через НАДН (никотинамидадениндинуклеотид).
Немаловажными видами антигипоксических препаратов являются вещества, которые стимулируют анаэробную выработку энергосубстратов в условия гипоксии. Энергосубстраты разделяются на 2 группы. Самый известный энергосубстрат – глюкоза, образованная путём гликолиза. К второстепенным энергосубстратам относят гексозы (глюкозо-фосфаты, фруктозо-дифосфаты). Способность глюкозы оказывать антигипоксический эффект ранее была обусловлена экономией своих макроэргов в клетках, растрачиваемых на процессы фосфорилирования фосфосахаров. Однако, на сегодняшний момент выявлено, что фосфорилированные углеводороды оказывают слабое влияние на устранение гипоксии. При разнообразных формах гипоксического состояния тканей были обнаружены лишь незначительные положительные изменения от использования фосфосахаров. Выявлено, что антигипоксическая активность разнообразных фосфосахаров практически неотличима друг от друга. Предполагается, что клеточные оболочки защищены от проникновения всех метаболитов гликолиза, что понижает значимость данных веществ при воздействии гипоксии.
По всей вероятности, при надобности приёма данного подкласса препаратов для каждого спортсмена в индивидуальном порядке принимается решение о парентеральном введении глюкозы с инсулином. Внутривенное использование раствора глюкозы вместе с инсулином при нарушениях работа миокарда предотвращает дальнейшие повреждения тканей сердца при недостаточном содержании кислорода в них.
Эффект, отмечающийся при использовании поляризующей смеси, который основан на регуляции метаболических процессов в миокарде (связанных с воздействием гипоксии) и на смене источника энергообеспечения (с маловыгодного для тканей окисления жиров на гликолиз), более целесообразен для поддержания работы сердца при недостатке кислорода. Сердце в условиях гипоксии является хорошим объектом для подобного лечебного воздействия, так как даже в нормальном состоянии 25% от всего количества кислорода в нём растрачивается на гликолиз, другая часть кислорода участвует в окислении жирных кислот и выведению молочной кислоты. Установлено, что использование поляризующей смеси во время инфаркта миокарда подавляет окислительные процессы в сердечной мышце и усиливает взаимодействие глюкозы с тканями сердца.
Для увеличения отдачи от процесса гликолиза для усиления кардиопротекторного воздействия поляризующей смеси рекомендуется использовать магний и калий глюконат, которые являются стимуляторами окислительных процессов глюкозы. Калия и магния глюконат предназначен для использования как в ходе выполнения тренировочного плана, так и в соревновательный период. Парентеральное использование глюконата и смеси задействует транспортную систему красных кровяных телец (эритроцитов), которая будет переносить кислород за счёт кумуляции глицеральдегида и фосфоглицерата, что в свою очередь происходит одновременно со стабилизацией уровня кислорода. Данное средство используется орально для усиления адаптационных процессов, необходимых для нормальной работы сердечно-сосудистой и дыхательной систем в тренировочный период. При возникновении необходимости в повышении кислородной ёмкости вероятно парентеральное введение 10-%-ного раствора по 10 мл NaCl за 2 часа до физической активности.
Широкое использование препаратов с АТФ не имело смысла, поскольку АТФ очень быстро (в течение 2-х секунд) подвергался ферментации. Применение же АТФ в комбинации (к примеру, в препарате АТФ-Лонг) было уже на порядок эффективнее, так как его компоненты более устойчивы к воздействию ферментов и имеют пролонгированный эффект действия. Структура АТФ-Лонг в 2,5-3 раза стабильнее АТФ. Фармакологический эффект этого препарата, как правило, обусловлен его воздействием на рецепторы пурина в миокарде, что подавляет чрезмерный рост кальция и пролонгирует эффект от экзогенного АТФ. АТФ-Лонг оказывает значительный актопротекторный эффект, особенно при длительных и среднеинтенсивных нагрузках.
АТФ-Лонг увеличивает общую выносливость человеческого организма. Последние данные исследований установили, что длительное использование АТФ-Лонг повышает переносимость нагрузок и увеличивает скоростно-силовые характеристики спортсмена. Единичный приём данного препарата усиливает мышечную мощность при выполнении большого объёма физических упражнений, причём всё это не сопровождается чрезмерным ростом концентрации лактата в мышцах. При этом улучшается переносимость человека к физическому воздействию нагрузок. АТФ-Лонг принимается под язык по 10-20 мг за 2 часа до предстоящей тренировки. Прогресс в лечении гипоксии миокарда наблюдался при введении в терапевтическую практику лекарственных средств, содержащих искусственный фосфокреатин. Его основной функцией является поддержание внутриклеточной транспортировки макроэргов в мышечных клетках сердца, клетках поперечнополосатой мускулатуры, нейронах, клетках сетчатки и спермацитах. Фосфокреатин, содержащийся в мышечных клетках сердца в больших количествах, является показателем прочности мембранных оболочек. Низкий уровень этого вещества в клетках сердца во время гипоксии может дестабилизировать клеточные мембраны. Взяв за основу результаты нескольких широкомасштабных исследований учёные установили, что искусственный фосфокреатин, особенно, в повышенной дозировке, увеличивает количество макроэргов, повышает количество энергии в клетках, а также сохраняет целостность клеточных оболочек в повреждённых ишемией мышечных клетках. Предполагается, что протекторное воздействие фосфокреатина – достаточно сложный биохимический процесс, состоящий, как минимум, из 4-х этапов:
- Попадание фосфокреатина в клетку и его прямое участие в сохранении запасов АТФ;
- Подавление процессов разрушения нуклеотидов в сарколемме клеток сердца;
- Подавление кумуляции лизофосфоглицеридов в тканях сердечной мышцы во время гипоксии;
- Снижение коагуляции тромбоцитов за счёт элиминации АДФ (аденозиндифосфата) из клеток и повышение эластичности клеточных оболочек у эритроцитов в системе кровообращения.
Следовательно, при введении искусственного фосфокреатина отмечается снижение симптоматики ИБС, аритмии и активности процессов перекисного окисления липидов. Лекарственное средство, содержащее фосфокреатин – неотон – используется в кардиологической практике, к примеру, его часто применяют при возникновении ранней симптоматики инфаркта миокарда. Как правило, 2г. неотона вводится в кровь с его дальнейшей инфузией по 3 г. в час на протяжении 2-х часов. При необходимости также применяется поддерживающее лечение в течение следующей недели после появления инфаркта, количество вводимого препарата во время терапии – 5-10 г. в день. На фоне лечения отмечается нормализация кровообращения в области ишемического поражения сердца за счёт элиминации токсических метаболитов из органа.
В спортивной медицине фосфокреатин используется в качестве препарата-мобилизатора, ускоряющего метаболические и транспортные процессы в организме. Подробный план приёма – 3-4 г. фосфокреатина (неотона) за сутки до предстоящих состязаний.
Сложность применения неотона обусловлена введением препарата внутривенно, что как правило, запрещается всеми антидопинговыми организациями. В данном случае привлекательным считается приём украинского аналога – реотона, который можно применять перорально. В одной таблетке реотона находится 500 мг гидрофильного фосфокреатина в комбинации с АТФ и магнием. Данный препарат протестирован на спортсменах при работе на выносливость. На фоне приёма увеличились скоростно-силовые показатели и выросла активность регенерирующих процессов. Реотон принимается сублингвально по 2 таблетки 3 раза в сутки.
Несколько лет назад в странах Европы и США проводились исследования по применению янтарной кислоты в качестве антигипоксического средства, под воздействием которой существенно снижалась выраженность симптомов при гипоксическом ацидозе различной этиологии. Подобное воздействие, как правило, связано с макроэргическими эффектами сукцината. Итогом этого является рост выработки АТФ и замедление гликолитических процессов на фоне усиленного глюконеогенеза.
Расщепление сукцината является важным условием катаболизма любой из трикарбоновых кислот в качестве энергосубстратов. Данный факт был изложен Кребсом, установившим, что окисление трикарбоновых и дикарбоновых кислот имеет свою особую цикличность. Такое явления было названо в его честь – циклом Кребса или по-другому — циклом трикарбоновых кислот. В связи с этим, было обнаружено, что для поддержания клеточного дыхания достаточно наличия одной уксусной кислоты или ацетилкофермента-А, прочие энергосубстраты могут оставаться неизменными.
Сукцинат представляет из себя стимулятор выработки факторов клеточной регенерации. Установлено явление быстрого расщепления сукцината в цитозоле при воздействии на него соответствующего фермента сукцинатдегидрогеназы, итогом этого процесса является восстановление нуклеотидов. Процесс, наблюдаемый при включении в клетку молекул янтарной кислоты, стал называться монополизацией сукцинатом цепи окисления. Суть данного процесса состоит в краткосрочном ресинтезе АТФ в клетках и борьба с большим количеством свободных радикалов.
Самыми значимыми веществами, относящимися к регуляторам гипоксического состояния тканей, некоторое время назад являлись стимуляторы активности ферментов и коферментов. Эта подгруппа препаратов рассматривалась в качестве основной группы антигипоксических лекарственных средств, к которым ранее причислялись:
- Витамины из группы В – В1, В3, В6, В9, В12 и В15;
- Производные меркаптанов;
- Пиримидины.
Их использование в медицинской практике не показало значительной эффективности, в частности, при их применении для повышения работоспособности спортсменов. К примеру, для преобразования витамина В3 в НАД организм должен стимулировать реакции прямой выработки, активность которых спровоцирована дефицитом кислорода и, следовательно, антигипоксическое действие витамина В3 крайне мало и неэффективно. Витамин В1 является важным элементом дегидрогеназ, участвующих в декарбоксилировании пирувата и альфа-кетоглутаровой кислоты. Однако даже повышенные концентрации кофермента и витамина В1 в крови не способствуют их проникновению в клетку. Антигипоксический эффект комбинации витаминов В1, В2 и С выражен слабо.
Действие витамина В1 в качестве восстановителя может рассматривается из-за его способности регулировать скорость формирования молочной кислоты при недостатке инсулина, развивающего спустя 8-10 часов после высокоинтенсивной тренировки или же после окончания соревнования. В этом случае увеличение активности транскетолазной реакции под воздействием витамина В1 усиливает выработку пириновиноградной и молочной кислоты, а также ускоряет их элиминацию в цикле Кори.
Предполагается, что использование витамина В1 в комплексе с бетаином и глицином оправдано с точки зрения антигипоксического воздействия на ткани. Путём усиленного трансметилирования с учётом действия бетаина и формирования НАДФН (никотинамидадениндинуклеотидфосфата) алактон – препарат, содержащий глицин, тиамин и бетаин, уменьшает время восстановления после тренировочных нагрузок и снижает токсичность метаболитов, образовавшихся в тканях в условиях гипоксии, вдобавок, препарат оказывает гепатопротекторный эффект.
Большой интерес в плане антигипоксического эффекта представляют производные гуанилмочевины. Подобный класс препаратов, помимо стимуляции гликолиза, способствует снижению концентрации молочной кислоты внутри и снаружи клеток, а также в общем кровотоке и мышечной ткани (снижение количества лактата не осуществляется только в тканях печени). Результатом такого воздействия является нормализация кислотно-щелочного баланса в биожидкостях организма и устранение гипоксии. Ресинтез глюкозы в данном случае осуществляется не в цикле трикарбоновых кислот, а в цикле Кори.
Установлено, что производное тиомочевины – амтизолсукцинат показывает наибольшую активность при возникновении недостатка кислорода, обусловленного постоперационным состоянием либо инфарктом миокарда. Амтизолсукцинат не напрямую задействует регуляционную функцию гипоксических процессов. Дозировки данного вещества для коррекции сердечной гипоксии составляют – 3 мг на кг веса человека, более высокие дозировки назначаются при значительной гипоксии.
Амтизол оказывает прямое инотропное воздействие на сердце и может предотвращать чрезмерную коагуляцию при тромбофилии, недостатке кислорода и энергосубстратов. Плюс ко всему амтизол стабилизирует устойчивость мембран, что как раз связано со способностью препарата уменьшать активность перекисного окисления липидов.
Одним из регуляторов гипоксии также может являться гемолизат эритроцитов, который содержит большое количество полисахаридов, гликолипидов, АТФ, АФД, цАМФ и аминокислот. К основным таким препаратам относят – Актовегин, который используется в больших дозировках (2г в день) для профилактики патогенеза гипоксии. Препараты могут ускорить процессы восстановления тканей, поэтому их приём нередко практикуется спортсменами.
Ещё один препарат с аналогичным воздействием – коэнзим Q или убихинон – может предупреждать дальнейшее развитие гипоксии, в том числе и при его использовании на начальных этапах. Эффект от приёма этого препарата исключителен, поскольку, он может полностью восстановить функциональность головного мозга даже при 10-минутной остановке сердца. Не исключается тот факт, что действие данного лекарственного средства может быть обусловлено его антиоксидантным эффектом. При всех плюсах препарата, его приём при достаточно выраженной гипоксии оказывает менее существенное воздействие.
Основное действие этилтиобензимидазола в организме связано со стимуляцией синтеза РНК в соматических клетках, что способствует усилению белкового синтеза. Объясняется этот процесс взаимодействием препарата с ДНК, поскольку этилтиобензимидазол обладает структурной схожестью с азотистыми основаниями. Данное воздействие не является зависимым от типа тканей, при этом оно выражается намного более сильно в тех тканях, где быстрее реализуются процессы синтеза РНК.
Медикаментозные препараты-кардиопротекторы, действие которых основано на подавлении выработки свободных жирных кислот в мышечных клетках сердца – мельдоний и триметазидин назначаются только по предписанию врача в индивидуальном порядке. Их использование в качестве метаболизирующих препаратов может быть оправдано только в межсоревновательный и начальный тренировочный период, однако будет неуместно в соревновательное время. По сведениям последних клинических испытаний, триметазидин предотвращает развитие нарушений, связанных с обменными процессами на фоне ишемического состояния сердечной мышцы. Триметазидин ингибирует фермент, участвующий в перекисном окислении липидов – кофермент-А-тиолазу, что приводит к переключению энергопотребления в миокарде за счёт гликолиза с параллельным снижением числа свободных радикалов. При этом, необходимо упомянуть, что такие изменения способствуют кумуляции липидов в теле митохондрий. Используемый для предотвращения триметазидин поддерживает энергообмен в миокарде, корректирует ионный баланс в клетках сердца, предотвращает развитие ацидоза внутри самих клеток и подавляет кумуляцию натрия и кальция в кардиомиоцитах, тем самым угнетая деятельность свободных радикалов. При этом влияние лекарственного средства может быть неэффективным, если его применяют уже после развития гипоксии.
О воздействии триметазидина на физическую производительность у людей без отклонений по состоянию здоровья известно, что заблаговременное внутримышечное введение данного лекарственного средства в дозировке 50 мг\кг веса тела не оказывает какого-либо актопротекторного влияния. В авторитетных научных источниках недостаточно данных, описывающих эффективность использования данного препарата в тренировочной практике. Наряду с этим другие учёные предоставили противоположные результаты, которые были получены эмпирическим путём (триметазидин использовался в комбинации с препаратами магния на протяжении 15-20 дней в суточной дозировке 0.04 и 1 г у спортсменов-велосипедистов). В них говорилось о том, что это лекарственное средство можно рассматривать в качестве препарата выбора для предотвращения негативных изменений, обнаруженных на ЭКГ при воздействии на организм высокообъёмных и высокоинтенсивных нагрузок аэробного и анаэробного характера.
Мельдоний (милдронат) полученный химическим путём латвийскими учёными, представляет из себя мощнейший ингибитор гамма-бутиробетаингидроксилазы, снижающий степень окисления липидов за счёт подавления их транспортировки в митохондрии. Происходит это за счёт торможения прежде всего транспорта L-карнитина, обеспечивающего перемещение свободных жирных кислот сквозь клеточную оболочку. Мельдоний замедляет синтез L-карнитина из гамма-бутиробетаина. За счёт чего изменяется карнитин-зависимая транспортировка сложных липидов сквозь оболочку митохондрий. Ингибирование окислительных процессов с участием жирных кислот состоит из вспомогательных механизмов выработки энергии: происходит окисление простых сахаров, в том числе и глюкозы, что приводит к более эффективному потреблению кислорода для формирования молекулы АТФ. При всём при этом на сегодняшний момент остаётся неясным тот факт, как именно проявляет себя милдронат в качестве ингибитора карнитина, поскольку L-карнитин хорошо защищает клетки сердца от гипоксии.
Карнитин представляет из себя вещество, образуемое из метионина и лизина, имеет немаловажное значение в транспортировке сложных жирных кислот внутрь самих митохондрий, при этом простые жирные кислоты могут активизироваться и транспортироваться в клетки и без карнитина. Помимо этого, карнитин участвует в процессах формирования и контроля концентрации ацетилкофермента-А. Уровень данного вещества в крови зависит от увеличения уровня ферментов пириновиноградной кислоты, которые помимо расщепления пирувата, замедляют выработку молочной кислоты. Следовательно, его антигипоксический эффект, который обусловлен транспортировкой липидов в митохондрии, зависит от повышенных дозировок карнитина, наряду с тем, как сниженные дозировки имеют лишь витаминное воздействие на организм.
Принцип воздействия мельдония на физическую активность при нормальном состоянии здоровья изучен слабо. Установлено, что заблаговременное введение (за полчаса до предстоящей нагрузки) мельдония в дозировке 100 мг\кг не оказывало актопротекторного воздействия, также, как и при использовании триметазидина. Серьёзных работ, посвящённых оценке применения мельдония в спортивной медицине, практически нет. В одном из немногочисленных исследований утверждалось, что оральное использование мельдония велосипедистами в дозировке 1г за 3-4 часа до гонки приводит к задействованию в работу всех энергозапасов в мышечной ткани и небольшому росту VO2max, что также способствует увеличению аэробной производительности спортсмена. При этом, данную информацию не стоит рассматривать как убедительную за счёт маловероятности появления быстрых эффектов при оральном приёме.
Тиотриазолин оказывает антиоксидантный и антигипоксический эффект, нормализует мозговое кровообращение, усиливает кровоток в коронарных артериях и зрительной зоне.
Нужно также принять во внимание то, что использование антиоксидантов, к примеру, кверцетина, также оказывает защитное влияние на сердечную мышцу путём регуляции активности соответствующих ферментов. Подобного рода препараты увеличивают выработку NO, угнетают функциональность 5-липоксигеназы и выработку лейкотриенов, плюс ко всему, они нормализуют уровень кальция в крови.
Кверцетин – флавоноид, выпускающийся в гранулах, таблетированной форме и в виде раствора, предотвращает развитие окислительного стресса. Кверцетин обладает антиоксидантными и мембраностабилизирующими свойствами за счёт ингибирования циклооксигеназ, фосфолипаз и максимального подавления липооксигеназ. Препарат является профилактикой роста концентрации калия внутри клеток, оказывает защитное воздействие на внутренние стенки сосудов (такой факт прежде всего обусловлен возможностью препарата к высвобождению NO и ингибированием протеиновых ферментов). Пероральная форма препарата, в основном, предназначена для устранения симптомов стенокардии, а инъекции кверцетина (корвитина) используются в кардиологической практике при инфаркте миокарда. Выявлено также, что данное средство может положительно влиять на уменьшение области некроза.
Перорально кверцетин принимается по 1г – 3-4 раза в день.
Кардиопротекторное действие препарата усиливает липин – флавоноид, с антиоксидантным и мембраностабилизирующим действием, который также может приводить в норму концентрацию макроэргов. Липин также очень эффективен при проведении комбинированной терапии у пациентов с ИБС. При всём при этом воздействие кверцетина на организм полностью не исследовано.
Растительные кардиопротекторы, обладающие антиоксидантным эффектом восстанавливают нарушенный кровоток в коронарных артериях и нормализуют фракцию выброса. К таким средствам относят – экстракт боярышника и Кардиплант, нередко они назначаются при комплексной фармакологической терапии, направленной на лечение ИБС и другие кардиологических недугов.
Существенное антиаритмическое и противоишемическое воздействие на организм оказывает препарат под названием Кратал, который содержит в своём составе таурин в количестве 0.8 г, экстракт боярышника – 0.04 г. и экстракт пустырника – 0.08 г. Этот фитопрепарат ингибирует активность ренина, ангиотензина, кинин-калликреиновую систему, нормализует кровоснабжение в миокарде, поддерживает физиологический показатель фракции выброса, вдобавок к этому, на фоне применения Кратала наблюдается уменьшение кровяного давления и нормализация пульса.
Экстракт боярышника несущественным образом повышает сократительную способность миокарда и снижает его возбудимость. Эффекты от приёма препарата пустырника схожи с действием других успокоительных препаратов, которое в целом обусловлено тормозящим воздействием на центральную нервную систему. Предполагается, что экстракт пустырника также, как и валериана, оказывает ингибирующий эффект на распад ГАМК (гамма-аминомасляной кислоты). Таурин представляет из себя кардиотоническое средство мягкого действия, сохраняющее энергозапасы в мышцах для нормальной мышечной работы, вдобавок таурин прямым образом влияет на мышечные белки в сердце и на уровень кальция в кардиомиоцитах.
Таурин снижает токсический эффект от передозировки гликозидов, однако при этом усиливает их действие на энергозапасы.
Растительные препараты Кардиотон и Kardioton
Существенный кардиопротекторный эффект отмечается при использовании препарата «Кардиотон», в котором помимо боярышника, содержатся также магний, калий и витамин В9. Кроме непосредственного кардиотропного эффекта «Кардиотон» поддерживает концентрацию описанных микроэлементов в норме, тем самым снижая дистрофические изменения в сердечной мышце.
Отдельно можно выделить препарат «Kardioton», который снижает гипоксическое воздействие на клетки миокарда и препятствует гипертрофии левого желудочка.
Показания и противопоказания кардиопротекторов
Если вы решили попробовать препараты — кардиопротекторы, то должны знать, что они имеют как показания, так и противопоказания. К первой категории относится:
• нарушения ритмичности работы органа;
• нарушения в работе печени (цирроз, жировая дистрофия, гепатиты);
• хирургическое вмешательство на изолированной почке;
• хориоретинальные сосудистые нарушения;
• головокружения и др. болезненные состояния организма.
Что же касается противопоказаний к кардиопротекторам, то самыми главными являются: почечная недостаточность, нарушения в работе печени, повышенная чувствительность к компонентам, детский возраст, беременность и период лактации. Есть такие кардиопротекторы, которые нельзя принимать при подагре, гиперурикемии.
Классификация фармакологических кардиопротекторов
Ниже описаны фармакологические параметры некоторых препаратов с кардиопротекторными свойствами.
Мельдоний (милдронат) достаточно быстро усваивается, его показатель биодоступности – 75%, максимальное количество препарата в крови отмечается спустя 1-2 часа после однократного применения. Метаболизм препарата происходит с формированием 2-х метаболитов, выводящихся с мочой. Период полуэлиминации составляет – 3-5 часов.
Также достаточно быстро абсорбируются такие препараты как: рибоксин, таурин, АТФ-Лонг и прочие средства, улучшающие метаболические процессы в организме. Препараты, содержащие креатинфосфат – Ритмокор и Неотон оказывают схожий кардиопротекторный эффект, при этом, способы их введения неодинаковы. Неотон в виде раствора необходимо вводить внутривенно. При разовом введении данного препарата его максимальный уровень в крови отмечается спустя 1-3 минуты, период полуэлиминации Неотона – 4-8 часов (в зависимости от функций и здоровья почек). Большая часть активного вещества кумулируется в сердце, а
Способ применения кардиопротекторов
Кардиопротекторные средства, кроме того, что имеют определенные показания и противопоказания, для того чтобы достичь эффекта, должны правильно приниматься. Вот, к примеру, препарат Ангиозил ретард, выпускается в виде таблеток, покрытых оболочкой. Внутри каждой из них содержится по 35 мг основного действующего вещества, речь идет дигидрохлориде и триметазидине. Упаковки из 60 таблеток хватает надолго. Независимо от того, в каких целях (лечебных или профилактических) используется кардиопротектор, достаточно принимать 2 раза в день по одной таблетке. Принимать их нужно во время еды, а продолжительность терапии зависит от поставленной цели и общей клинической картины.
Если говорить о таком кардиопротекторе, как Тиотриазолин, который выпускается в форме таблеток и инъекций, то курс его применения очень зависит от поставленных лечебных целей. Например, при гепатите сначала в течение 5 дней вводятся по 2 мл раствора 3 раза в день, после чего назначается таблеточная форма. В течение дня больной должен принять 300 мг лекарства. Схемы приема определяются только врачом.